Как работают антипаркинсонические мутации
Мутантный микропротеин повышает стабильность энергетических белковых комплексов в митохондриях, помогая митохондриям сопротивляться вредным воздействиям.
Вероятность нейродегенеративных болезней – таких как болезнь Альцгеймера и болезнь Паркинсона – может повышаться от определённых мутаций, определённых вариантов генов. Самый известный пример – болезнь Альцгеймера и варианты гена APOE. Но точно также есть мутации, которые работают против «нейродегенеративок». Подобные мутации обнаруживают по мере изучения человеческого генома: в прошлом году мы узнали о новой антиальцгеймерической мутации, найденной в генах одной колумбийской семьи.
Есть защитные мутации и против болезни Паркинсона. Например, известно, что у людей с некоторыми вариантами митохондриальной ДНК «паркинсон» случается ощутимо реже; вообще связь митохондрий с болезнью Паркинсона опять же изучается давно. Митохондрии, которые дают клетке энергию, располагают собственным небольшим геномом и сами синтезируют некоторые белки, необходимые для энергетических реакций. Однако до сих пор не всегда понятно, каким образом та или иная мутация в митохондриальном геноме защищает от болезни Паркинсона.
Сотрудники Университета Южной Калифорнии сосредоточились на мутациях в митохондриальном микропротеине SHLP2. Микропротеинами называют особые небольшие белки, которые влияют на сборку крупных белковых комплексов. Молекулы белков в клетке часто объединятся друг с другом, потому что только в непосредственном контакте они могут выполнять свои функции. Получаются димерные, тримерные, тетрамерные и т. д. комплексы, которые к тому же могут состоять как из белков одного вида, так и из белков разных видов. Микропротеины как раз регулируют их сборку, и сами порой входят в состав этих комплексов в качестве небольшой, но важной детали.
Для начала исследователи проверили, действительно ли у SHLP2 есть антипаркинсонические свойства. Для этого последовательность митохондриальной ДНК, соответствующей SHLP2, сравнили у нескольких тысяч людей, как здоровых, так и заболевших «паркинсоном». В результате удалось выявить вариант SHLP2, с которым вероятность получить болезнь Паркинсона уменьшается примерно вдвое. Особенность этого варианта – замена одной-единственной аминокислоты, из-за чего весь микропротеин становится намного более стабильным, чем другие его варианты.
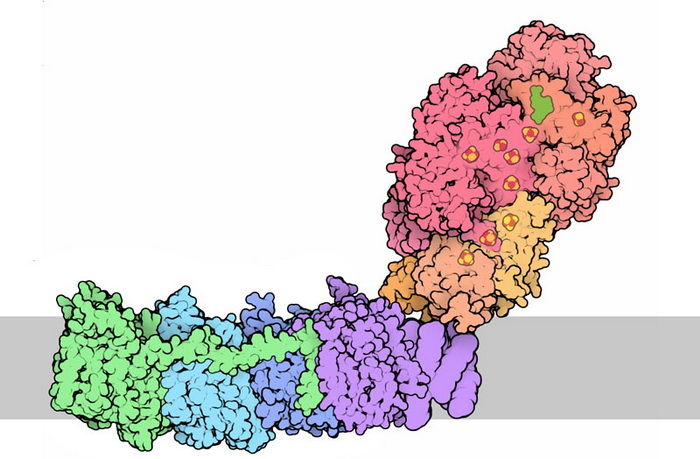
НАД-дегидрогеназный комплекс, или комплекс I, расположенный во внутренней мембране митохондрии. Цветами показаны некоторые белковые субъединицы в его составе. Иллюстрация: David Goodsell & RCSB Protein Data Bank / Wikipedia
SHLP2 работает с митохондриальным комплексом I, или НАДН-дегидрогеназным комплексом. Сам комплекс – часть цепи переноса электронов. Электроны отрываются от, условно говоря, питательной молекулы; перебрасывая электроны друг другу, белки электронтранспортной цепи перекачивают ионы водорода (протоны) с одной стороны мембраны на другую. На мембране образуется протонный градиент, который запускает фермент, синтезирующий АТФ, главную энергетическую молекулу клетки. Комплекс I состоит у млекопитающих из 44 субъединиц, то есть из 44 отдельных полипептидных цепей. В Molecular Psychiatry говорится, что антипаркинсонический SHLP2, будучи сам более стабильным, повышает устойчивость комплекса I, усиливает его способность сопротивляться разным неприятностям. В экспериментах с мышами и в экспериментах с человеческими нейронами использовали токсин, вызывающий паркинсонические изменения в клетках, действуя на митохондриальный комплекс I. Защитный вариант SHLP2 помогал комплексу оставаться целым и работоспособным; вместе с ним продолжали работать и митохондрии.
Вариант SHLP2, о котором идёт речь, встречается только у 1% людей (по крайней мере, если брать европейцев), но, может быть, его действие можно сымитировать, или просто синтезировать его искусственно, чтобы использовать как лекарство. Нарушения в комплексе I наблюдаются не только при болезни Паркинсона, но и при других возрастных заболеваниях, так что какое-нибудь SHLP2-подобное лекарство нашло бы применение не только в лечении нейродегенеративных расстройств. Хотя есть и другие подходы: прошлой осенью мы писали, что болезнь Паркинсона можно остановить, простимулировав в нейронах уборку клеточного мусора – испорченные митохондрии просто уйдут из клеток, перестав им вредить. Правда, те эксперименты ставили опять же на мышах.



