Осмий
В периодической таблице существует неофициальная группа самых-самых элементов, своего рода рекордсменов по определённому свойству. По какому параметру сравнивать элементы – выбор, на самом деле, весьма большой. Можно искать самые редкие элементы, самые дорогие или даже элементы с самым длинным названием. Последнюю номинацию, кстати, делят между собой целых три элемента: протактиний, резерфордий и дармштадтий. Мы же поговорим об элементе с самой большой плотностью, и это совсем не уран или ртуть, а элемент с порядковым номером 76 – осмий.

Искусственно выращенные кристаллы чистого осмия. Фото: GrrlScientist/Flickr.com CC BY 2.0
Конечно, если говорить строго научным языком, то у элемента не может быть плотности, потому что элемент - это название определённого типа атомов. А плотность и множество других свойств появляются уже у вещества – объединения хотя бы нескольких атомов. Когда вместе объединяются атомы одного вида, то такое вещество называется простым. Например, если мы соберём вместе много атомов золота, то получим тоже золото, но уже в виде драгоценного металла жёлтого цвета. Путаница возникает из-за того, что элемент и простое вещество называются одинаково, хотя за одним и тем же названием стоит разный смысл. Так и с осмием, самую большую плотность, которая более чем в полтора раза больше, чем у ртути, имеет именно простое вещество осмий, а совсем не элемент. Обычно химики не любят уточнять, что они имеют в виду: элемент или простое вещество, считая, что это и так очевидно из контекста. Хотя в некоторых случаях, когда обе трактовки по смыслу кажутся вполне допустимыми, с первого раза бывает не просто разобраться, о чём же идёт речь. Вооружившись этим небольшим ликбезом по химической терминологии, вернёмся к нашему осмию.

Природный минерал, содержащий металлы платиновой группы: осмий, иридий, рутений и родий. Фото: D. Nishio-Hamane/Flickr.com CC BY-NC-SA 2.0
Как мы уже сказали, у осмия самая высокая плотность из всех известных веществ. А знаете, что попробует сделать настоящий исследователь, если ему дать самый плотный в мире металл? Разумеется, он попытается уплотнить его ещё больше! И у этого занятия помимо исследовательского азарта есть и вполне конкретный научный интерес. Всё дело в том, что при очень высоких давлениях обычные вещества могут непредсказуемо менять свои свойства. Например, блестящий металлический натрий превращается в прозрачный диэлектрик, газообразный кислород, наоборот, затвердевает и даже становится сверхпроводником. Всё это открывает окно в уникальный мир сверхвысоких давлений, которые существуют, к примеру, в ядрах планет. Чтобы не лезть за сверхвысоким давлением в самый центр Земли, исследователи придумали интересный инструмент – алмазную наковальню. Благодаря исключительной твёрдости алмаза между двумя его поверхностями можно создать колоссальное давление, даже в два раза большее, чем в центре Земли. А за счёт его прозрачности сквозь алмазные наковальни можно в прямом смысле посмотреть, что же там происходит с исследуемым веществом. Так что же произошло с осмием, когда его сжали с давлением почти восемь миллионов атмосфер? Самое удивительное, что практически ничего – осмий сохранил свою кристаллическую структуру и все остальные свойства, попутно получив ещё один «приз» в номинации «самое устойчивое к давлению простое вещество».

Детали алмазной наковальни. Фото: Dawn Harmer/SLAC CC BY-NC-SA 2.0
Кроме максимальной плотности у осмия есть ещё одно примечательное свойство: у него очень высокая температура плавления, выше трёх тысяч градусов. Это позволило изготавливать из осмия спирали для ламп накаливания в самом начале прошлого века, пока осмий почти полностью не был вытеснен ещё более тугоплавким вольфрамом. Тем не менее, единство и борьба осмия с вольфрамом в ламповых спиралях нашли отражение в названии известной компании OSRAM, которая и по сей день выпускает самые различные осветительные устройства. Как вы уже могли догадаться, название состоит из частей названий этих двух элементов: ОСмий и вольфРАМ. Интересно, что для нашего языка, как и для немецкого, такое сокращение вполне понятно, а вот для англоговорящих стран «вольфрамовый след» уже не столь очевиден, потому что в английском языке вольфрам называется tungsten.

Спираль для ламп накаливания когда-то изготавливали из осмия и его сплавов с вольфрамом. Фото: Caleb Roenigk/Flickr.com CC BY 2.0
Помимо ламп накаливания, которые уже уступили своё место светодиодам, осмий использовали ещё в одном очень популярном, но теперь уже практически вышедшем из употребления предмете: перьевой ручке. Однако так же как светодиоды сейчас «убивают» классические лампы, так и шариковые ручки когда-то безжалостно оборвали золотой век ручек перьевых, оставив для них лишь узкую нишу ценителей оригинального письма. Если вы когда-нибудь держали в руках перьевую ручку, то могли заметить кончике пера небольшой шарик. Вот именно в нём и можно отыскать осмий и другие ценные металлы. Сам шарик нужен для того, чтобы перо могло гладко скользить по листу бумаги, не царапая его и не цепляясь за бумажные волокна. Однако если этот шарик сделать из той же стали, что и остальные части пера, то он очень быстро придёт в негодность. Если для дешёвых ручек это ещё хоть как-то простительно, то для дорогих перьевых ручек такая ситуация категорически недопустима. Поэтому шарик на кончике пера изготовляли из твёрдых сплавов, в том числе осмия, иридия и других металлов платиновой группы. Кстати, один из природных сплавов осмия с иридием называется иридосмин или минерал невьянскит, по названию Невьянска, города на Урале.

У качественных ручек наконечник пера изготавливается из твёрдых сплавов, содержащих осмий или другие металлы. Фото: János Fehér/Flickr.com CC BY-SA 2.0
Коль скоро мы коснулись темы пишущих принадлежностей, то хотелось бы рассказать об одном мифе, пусть и не связанным с осмием. Вы наверняка слышали такую историю, смысл которой состоит в том, что специалисты NASA потратили уйму средств и времени на изобретение ручки, которая может писать в невесомости, в то время как смекалистые русские космонавты продолжали использовать карандаш. Во-первых, до второй половины 1960-х годов и американские астронавты и советские космонавты использовали карандаши. Однако потом частный изобретатель Пол Фишер разработал специальную ручку, которая пишет в невесомости и в других экстремальных условиях. После чего предложил NASA опробовать своё изобретение взамен карандашей и фломастеров. Секрет ручки Фишера в том, что её пишущий шарик, выполненный из карбида вольфрама, прецизионно установлен в наконечнике стержня, чтобы избежать протекания. Чернила тиксотропны — твёрдые в обычном состоянии, они разжижаются только при письме. Сами чернила находятся в специальном картридже под давлением сжатого азота, который отделён от чернил скользящим поплавком. Так зачем же было изобретать такую сложную конструкцию, если вот оно простое решение – карандаш? Дело в том, что карандашам свойственно ломаться, и если в обычной жизни мы просто смахнём обломки со стола, то в невесомости они начнут жить своей жизнью, свободно летать по пространству космического корабля или станции, рискуя при этом попасть человеку в глаз.

Космическая ручка всё-таки лучше и безопаснее карандаша. Фото: James Fee/Flickr.com CC BY-NC-ND 2.0
Кстати, сам осмий получил своё название благодаря неприятному запаху, который описывают как смесь запахов хлорки и чеснока. Неприятное амбре возникает за счёт окисления осмия на воздухе, в результате чего образуется летучее соединение – тетраоксид осмия. Называть открытый в 1803 году элемент «чесночием» английский химик Смитсон Теннант, видимо, посчитал слишком легкомысленным, поэтому за основу названия он выбрал слово «запах» в греческом переводе. Учти он ещё и чрезвычайную ядовитость тетраоксида, осмий мог бы получить и более зловещее название. Но даже несмотря на высокую стоимость и опасность, это соединение всё равно находит своё применение в химических лабораториях. Например, его используют при синтезе кортизона – гормонального лекарственного средства или при химической обработке образцов для электронного микроскопа.
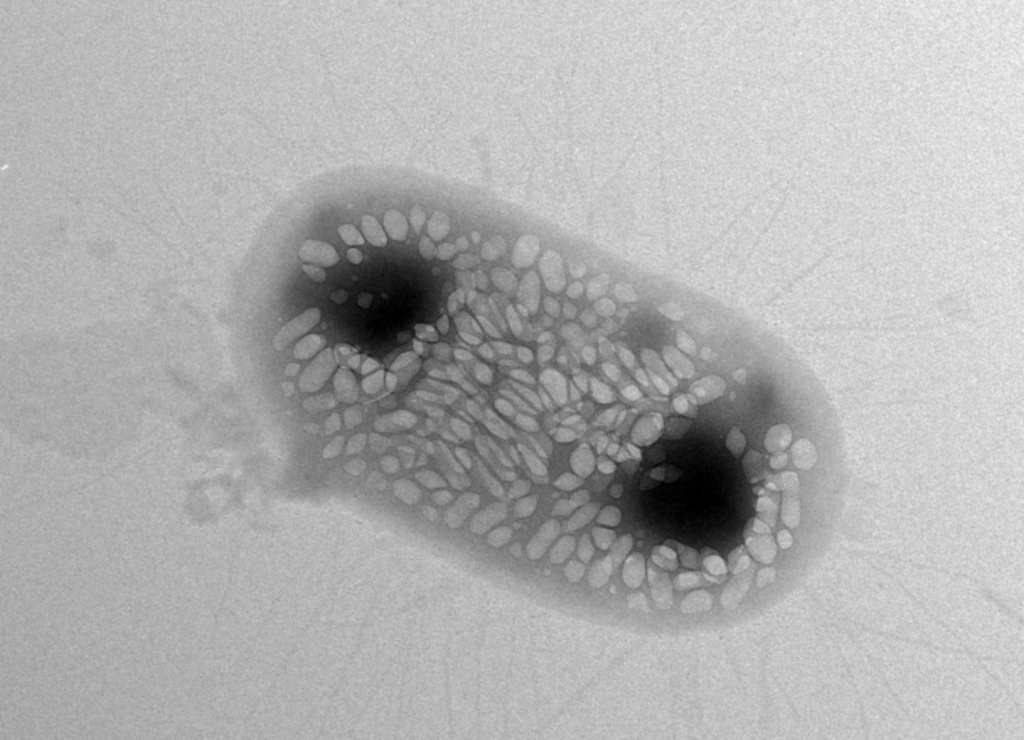
Чтобы получить изображение биологического объекта с помощью просвечивающего электронного микроскопа, его подвергают специальной обработке, где на одной из стадий используется раствор тетраоксида осмия. На фото изображена генетически модифицированная бактерия кишечной палочки. Фото: Anupama Lakshmanan/Caltech/Flickr.com CC BY-NC 2.0
Есть ещё одно место, где можно повстречать осмий, правда, это будет совсем не тот осмий, о котором мы говорили всё это время. Так уж сложилось, что один из родов пчёл получил название «осмии». Пчёлы этого рода ведут по большей части одиночный образ жизни, не образуют ульи и не производят вкусный мёд. Тем не менее, они прекрасно справляются с опылением растений, поэтому некоторые садоводы специально привлекают осмий на свои участки. Так что если вам когда-нибудь повстречается объявление со словами «продам осмий, дёшево», не обольщайтесь – вместо драгоценного металла, вам продадут милых пчёл из семейства мегахилиды. Не запутайтесь в том, что скрывается под словом осмий: элемент, простое вещество или… пчела!

#осмий #Менделеев #химия #периодическаясистема #элементы





